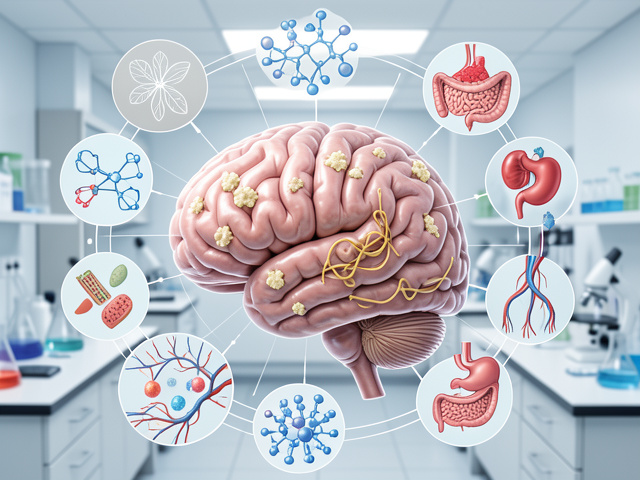
Алцхајмеровата болест со години се истражуваше претежно преку една главна хипотеза: дека наслагите од амилоид-бета се клучниот двигател на болеста. Но нов преглед на научни трудови укажува дека таквиот пристап е премногу тесен. Истражувачите предупредуваат дека Алцхајмеровата болест не е резултат на еден единствен механизам, туку на сложена мрежа од биолошки процеси поврзани со стареењето, генетиката, метаболизмот и општата здравствена состојба.
Во анализата, објавена во списанието Science China Life Sciences, тим предводен од професорот Јан-Џијанг Ванг посочува дека досегашните терапии насочени кон само една цел даваат ограничени резултати. Иако поновите лекови, како леканемаб и донанемаб, покажуваат дека може умерено да се забави когнитивното опаѓање, тие не ја враќаат нормалната функција на мозокот ниту ја запираат болеста.
Според авторите, покрај амилоид-бета, важно место има и протеинот тау. Кога тау претрпува патолошки промени, се создаваат заплеткани структури во нервните клетки, што е поврзано со нивно оштетување и умирање. Затоа, идните третмани веројатно ќе треба истовремено да ги таргетираат и амилоид-бета и тау, наместо да се потпираат на една биолошка мета.
Голема улога има и наследниот ризик. Најпознат генетски фактор е варијантата APOE ε4, но научниците идентификуваат и други генетски варијации што можат да влијаат на ризикот кај различни популации. Во тој контекст се разгледуваат и технологии за уредување на геномот, како CRISPR/Cas9, кои во иднина би можеле да понудат подиректно влијание врз корените на болеста. Засега, ваквите пристапи се во истражувачка фаза.
Прегледот посебно го нагласува стареењето како најсилен ризик-фактор. Со возраста доаѓа до слабеење на митохондријалната функција, акумулација на оштетени клетки и зголемено оштетување на ДНК. Научниците затоа разгледуваат и таканаречени сенолитички терапии, чија цел е отстранување на старите и нефункционални клетки што придонесуваат за воспаление и нарушување на мозочната средина.
Но Алцхајмеровата болест, според овој пристап, не треба да се гледа изолирано само како нарушување на мозокот. Инсулинската резистенција, високиот крвен притисок и промените во цревната микробиота исто така можат да влијаат врз развојот и текот на болеста. Поради тоа, се испитува дали некои постојни терапии за дијабетес, како и интервенции насочени кон врската меѓу цревата и мозокот, би можеле да имаат дополнителен ефект во намалување на ризикот или забавување на напредувањето.
Истражувачите сметаат дека следниот чекор е интегриран модел на лекување, во кој повеќе механизми ќе се третираат паралелно. Тука влегуваат и попрецизни дијагностички алатки, како рани биомаркери во крвта, меѓу кои pTau217, што би можеле да овозможат побрзо откривање на болеста и порано започнување на терапија. Дополнително, лабораториски модели како органоиди добиени од човечки iPSC-клетки би можеле да помогнат во подобро тестирање на нови терапии.
Главната порака од прегледот е дека Алцхајмеровата болест не може успешно да се контролира со еднодимензионален пристап. Ако болеста навистина произлегува од повеќе меѓусебно поврзани процеси, тогаш и третманот ќе мора да биде повеќеслоен. Наместо потрага по едно чудотворно решение, научната насока сè повеќе се движи кон комбинации од терапии, рана детекција и персонализирана медицина.