Развојот на нови лекови често запира уште во раните фази, бидејќи многу молекули не се однесуваат очекувано во биолошка средина. Истражувачки тим од Универзитетот во Орегон претстави пристап што со помош на вештачка интелигенција и физички модели предвидува како нови, претходно невидени молекули ќе се движат и ќе интеракцираат во организмот.
Наместо класични, многу скапи и пресметковно тешки симулации, моделот нуди побрз „среден пат“: доволно детални информации за клучните механизми, но со значително помал трошок на време и ресурси. Целта е научниците порано да препознаат кои молекули имаат реален потенцијал и кои не вреди да продолжат кон скапи лабораториски и клинички проверки.
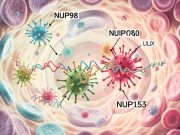
Методот е обучен со податоци за познати молекули, вклучувајќи и енергетски параметри за промени на нивната форма. Со тоа, алгоритмот не „лута“ низ малку веројатни сценарија, туку се фокусира на патеки што се физички веродостојни. Дополнителни математички техники ја зголемуваат шансата да се „уловат“ ретки, но критични моменти, како врзување на молекулата за целниот протеин.
Резултатите се објавени во Proceedings of the National Academy of Sciences (2025), во трудот „Data-driven enhanced sampling of mechanistic pathways“ (DOI: 10.1073/pnas.2517169122). Истражувачите најавуваат и следен чекор: резултатите да се претворат во појасни, визуелни прикази што ќе им помогнат на биолозите и хемичарите полесно да ги толкуваат симулациите.
Кодот е јавно достапен, што може да го забрза користењето на методот и во други области, од дизајн на материјали до пошироки биомолекуларни истражувања. Ако ваквите алатки продолжат да се развиваат, раната селекција на кандидат-лекови би можела да стане побрза, поевтина и попрецизна.